研究テーマ

千葉大学大学院医学研究院
呼吸器病態外科学
千葉大学病院
呼吸器外科

-末梢肺癌の確定診断のために-
1955年、当科において気管支鏡下のブラシ法を開発して以来、それまでは難しかった末梢の肺癌の診断が可能となりました。最初の診断率は60%程度でした。その後気管支鏡や器具の開発、改良を重ねたところ、今では針生検、鉗子生検などを加え、90%近くの末梢肺癌を術前に診断できるようになっています。
しかし、胸部CTなど画像診断も進歩したためかつては発見できなかったような2・未満の末梢小型肺癌の発見が可能となりました。これらの術前診断のために、1999年より通常使用する電子気管支鏡の半分以下の細さの気管支鏡(極細径気管支鏡)を導入しました。それまではレントゲンの透視のみで確認していた末梢の陰影も直接気管支鏡でみながら生検することが可能になりました。
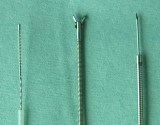
使用している鉗子
また、極細径気管支鏡では使用できない針鉗子が、使用できるやや細い気管支鏡(細径気管支鏡)も開発し、これらを症例によって使い分けています。
これら最先端の気管支鏡および器具を開発、使用することにより、末梢の肺癌の診断率は向上しており、全体では90%近く、早期に発見された小型肺癌でも 80%を超える診断率を誇っています。
気管支腔内超音波検査法は、気管支腔内に細径超音波プローブを挿入し、気道壁及び壁外の組織の断層像をえる検査法です。1990年代に入り本検査法が実用化され、超音波端子装置の軽量・小型化に伴い近年普及し、EBUSの臨床的有用性がますます高まってきています。現在は呼吸器領域の多くの疾患への診断、評価に応用されるようになってきました。気道壁および気管支周囲構造を観察する方法以外にも、肺末梢病変の経気管支肺生検のガイドおよび画像診断の手段として応用され良好な成績が報告されています。超音波プローブには気道の長軸方向のスキャンを行なうconvex typeとradial scanning transducerを備えたものがありますが、気管内に挿入するためあまり太い径のエコーは実用的でないこと、気管支鏡チャンネルを通過できることが理想であるためradial scanningのものが主として開発されてきました。一方、われわれは2002年より肺門・縦隔病変に対する低侵襲で確実な生検法としてEBUSガイド下にリアルタイムの経気管支針生検 (Real time endobronchial ultrasonography guided TBNA、 EBUS-TBNA)が可能であるコンベックス走査式超音波気管支鏡(convex probe EBUS : CP-EBUS)の開発に取り組んできました。
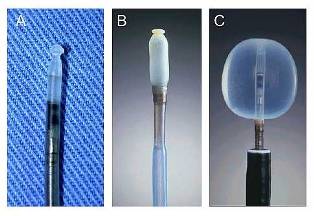
図1
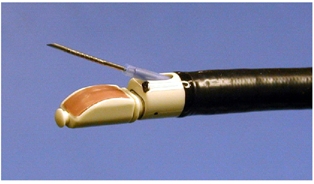
図2
気管支壁への腫瘍進達度とリンパ節腫大の評価には図1のようなラジアル走査式超音波プローブを使用しています。このプローブを気管支内の腫瘍にあてて、腫瘍がどの程度の深さまで浸潤しているかを決めることができます。
一方、図2は気管・気管支周囲病変に対するEBUS-TBNAが可能であるコンベックス走査式超音波気管支鏡で先端にlinear probeが装着されたビデオ気管支鏡です。
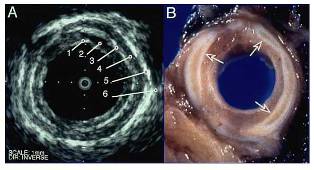
図3
気管支の正常エコー像は図3のように描出されます。
軟骨部では気管支内腔側からゴム性のバルーン(第1層),気管支軟骨への移行層(第3層),気管支壁外層への移行部(第5層)が高エコー層として描出されます。この高エコー層とそれに続く低エコー層で示される軟骨層を明瞭に描出すれば、気管支壁の構造は確実に把握できます。
またエコープローブの位置により気管支壁外にさまざまな構造物が描出されます。肺動脈・肺静脈の各分枝,大動脈,左心房,食道などが描出されるため、腫瘍とこれらとの位置関係や浸潤の有無をある程度把握することが可能です。
上の正常構造をもとに異常所見を判定します。
1)右上葉気管支発生扁平上皮癌
気管支鏡所見では右B3をほぼ完全閉塞する腫瘍を認め、気管支エコーを右B3に挿入し観察したところ腫瘍が軟骨輪を超えて壁外へ浸潤していることがわかります(図4)。
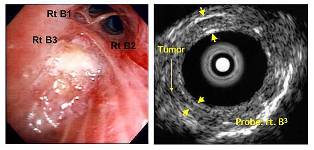
図4
2)左上葉上大区支原発扁平上皮癌
気管支鏡所見では左上葉上大区支に粘膜の不整を伴う小病変を認め、気管支エコーでは軟骨層が保たれており粘膜浸潤に留まると判断されました(図5)。
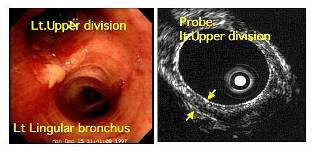
図5
コンベックス走超音波気管支鏡の開発により、気管・気管支周囲病変に対するリアルタイムの超音波ガイド下生検が可能となりました。
1)検査手順
肺癌症例における縦隔・肺門リンパ節の評価の場合には、末梢より両側の肺門リンパ節(#12、#11、#10)、縦隔リンパ節(#7、#4、#3、#2、#1)を順に観察し、リンパ節の有無を確認します。病変の穿刺には専用の22G吸引生検針を使用します。当施設では全例乾燥標本をDiff-Quik染色後、迅速細胞診を行っています。これにより、確実に細胞が採取されていることが確認でき、診断率の向上に役立ちます。また組織検体も採取されるため、組織学的な検討も可能です。
2)適応疾患
気管或いは気管支に接している病変であれば、EBUS-TBNAは可能です。現在まで施行した症例より、適応疾患には肺門・縦隔リンパ節腫脹症例、肺腫瘍、縦隔腫瘍などが挙げられます。
3)検査成績
肺癌症例
胸部CT上肺門・縦隔リンパ節腫脹を認める肺癌術前109症例においてEBUS-TBNAによるリンパ節転移診断を行った結果、106例でEBUS-TBNAが可能でした。EBUS-TBNAによる各症例のリンパ節stagingにおける診断では、感度93.3%、特異度100%、正診率95.3%であり、非常に高い診断率が得られました(図6)。また、このうち20症例は原発巣の診断未確定症例であり、リンパ節より確定診断が得られました。EBUS-TBNAにより、縦隔鏡、CTガイド下生検、開胸生検など多くの侵襲的は手技を回避することもできました。
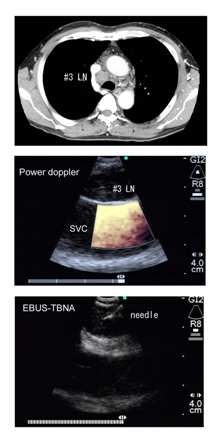
図6
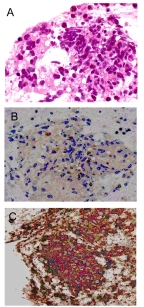
図7
縦隔腫瘍
原因不明縦隔リンパ節腫脹症例や縦隔腫瘍も診断が可能です。とくにサルコイドーシス症例は通常の検査法(TBLB、BAL等)では確定診断の得られなかった65例中において91.8%と非常に高い診断率を得ました。縦隔嚢胞については超音波画像上tumorとfluidの鑑別は容易であり、さらにカラードップラー併用により画像診断も可能です。内部の嚢胞液を吸引することにより縦隔嚢胞の診断が得られます。嚢胞液の生化学的検査への提出も診断に有用です。
一方、悪性リンパ腫の診断は細胞診だけではcell typeまで同定することは困難ですが、われわれの経験でも組織が十分採取された症例では免疫染色も可能であり、確定診断のうえ治療に移行することが可能でした(図7)。
4)EBUS-TBNAの限界
現行のCP-EBUSは挿入部先端部外径が6.9mmであることから、描出、穿刺できる病変が限られています。リンパ節については、葉気管支間リンパ節(#11)までは描出可能ですが、葉気管支周囲リンパ節(#12)は場所により、描出或いは穿刺が困難な場合もあります。また、食道傍リンパ節(#8)、肺靭帯リンパ節(#9)、大動脈下リンパ節(#5)、大動脈傍リンパ節(#6)等の気管支と接していないリンパ節について穿刺はできません。
さらに、専用の穿刺針は22Gと細く、19G Wang needleなどと比較すると、検体採取量は少なく、とくに縦隔腫瘍など、組織診断が必要となる症例においては、組織検体は必須であり、今後穿刺針の改良が望まれます。
蛍光気管支内視鏡は気管支鏡を通して青色光を気管支組織に照射し、正常気管支組織および癌など異常組織から発せられる自家蛍光の差を利用して、気管支の早期肺癌のなかでも上皮内癌やsquamous dysplasiaなどpreinvasive bronchial lesionと呼ばれる病理組織学的に気管支上皮層の基底膜を越えない微小な気管支病変を正確に診断するものです(図8)。
われわれは、当初Xillix社製LIFE-Lung Systemを用いて評価を行ってきました。主に重喫煙者を対象とした肺癌集検における喀痰細胞診にて悪性細胞や悪性細胞を疑う異型細胞が認められる症例に蛍光気管支内視鏡を施行することで、今までの気管支鏡単独では発見不可能であった微小な気管支病変が多数発見されるようになってまいりました。 蛍光気管支内視鏡では、正常気管支組織は緑色、癌をはじめとする病変組織は暗赤色としてTVモニターに画像化され異常組織の確認がなされます(図9)。
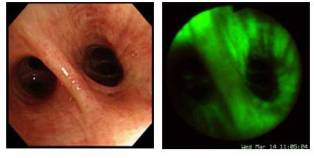
図8
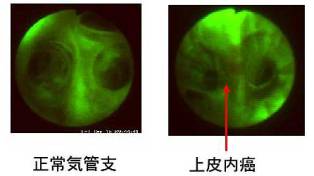
図9
現在われわれは、喀痰細胞診にて悪性細胞や悪性細胞を疑う異型細胞を有する患者さんから前癌性病変であるsquamous dysplasiaを確実に診断し、未だ癌へと進展していない状態での経過観察を行っております。また微小な扁平上皮癌と診断された患者さんに対しては、積極的に内視鏡的治療を施行しています。
さらに次世代の蛍光気管支鏡が開発され、現在はオリンパス光学の新しい自家蛍光電子内視鏡システム(AFI: Auto fluorescence imaging bronchovideoscope system)を使用しております。新しいAFIでは、気管気管支の粘膜病変の評価の際に、ヘモグロビン由来の蛍光減弱と上皮の肥厚などによる蛍光減弱が異なる色調で観察できます。すなわち、炎症や出血は青色の色調で描出されるため、癌やsquamous dysplasiaなどとは区別可能であり除外することができます(図10)。
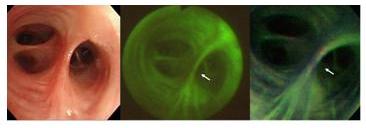
図10
拡大気管支鏡・NBI
拡大気管支ビデオスコープは、気管支鏡として許容できる6mmの外径で、観察深度は1-3mm、倍率は最近点で110倍観察となり、 TVモニターを通して気管支粘膜の詳細な観察が可能となりました。上皮下における微細な血管網を詳細に観察した結果、扁平上皮癌の前癌性病変と考えられているsquamous dysplasiaにおいて正常あるいは気管支炎に比べ血管網の増生、蛇行、錯綜が顕著に認められました(図11)。
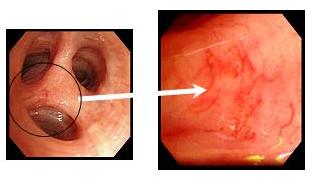
図11
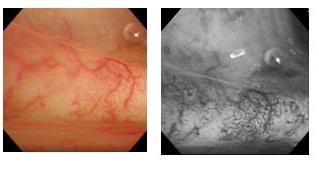
図12
さらに面順次式電子スコープの光源装置filterを、Blue1:400-430nm、Blue2:420-470 nm、Green:560-590 nmの狭帯域フィルターに変更したNarrow Band Imaging (NBI)を用いることで、squamous dysplasiaにおいて、NBI-Blue1画像では詳細な微細血管、微細血管網、点状血管の観察が可能となりました。点状血管は、形態計測の結果angiogenic squamous dysplasia(ASD)におけるcapillary loopの径と一致し、扁平上皮癌の多段階におけるangiogenesis を内視鏡的に捉えることに成功しました(図12)。