第3項先進医療(高度医療)
「非小細胞肺癌に対するNKT細胞を用いた免疫細胞治療(Chiba-NKT)
症例登録は終了しました。御協力ありがとうございました。
【概要】
これまで千葉大学が中心となり推進してきたNKT細胞を用いた免疫細胞治療の臨床開発研究の成果を踏まえて、平成24年1月に第3項先進医療(高度医療)「非小細胞肺癌に対するNKT細胞を用いた免疫細胞治療(Chiba-NKT)」として承認・告示され、肺癌を対象にしたNKT免疫細胞治療が標準治療に向けて第一歩を踏み出しました。千葉大学未来医療教育研究センター(平成24年1月発足)と千葉大学医学部附属病院臨床試験部を中心に臨床研究が推進され、実際の治療は千葉大学医学部附属病院呼吸器外科で行われます。
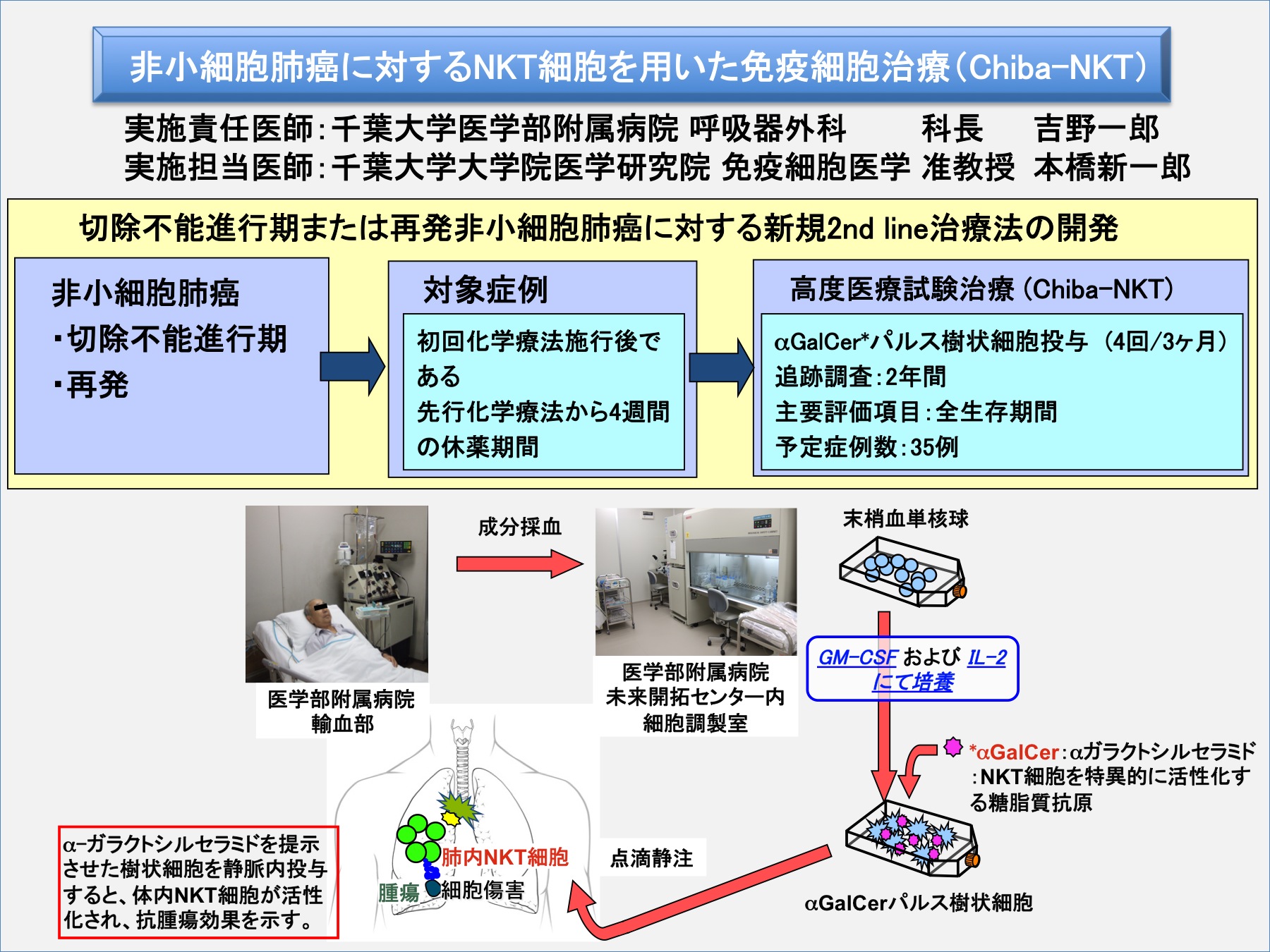
【背景】
原発性肺癌は全悪性腫瘍による死亡の約20%を占め、2009年では約6.7万人が死亡している。根治を目指した治療法は外科治療のみであるが、肺癌発見時に手術適応となるのは約3割に過ぎず、肺癌全体の5年生存率は25〜30%と言われている。切除不能進行期肺癌や肺癌術後再発の治療は主に抗癌剤による全身治療が中心となる。新規抗癌剤や分子標的薬の開発などにより、進行・再発肺癌の治療成績は徐々に向上しているものの依然完治は望めず、治療成績は未だ満足できるものではない。
日本では薬事法の承認が得られていない医薬品の使用を伴う先進的な医療技術は保険との併用が認められていない。しかし一定の要件を満たすものについては厚生労働省が「高度医療」として認め、保険診療と併用できることとし、薬事法による申請等に繋がる科学的評価可能なデータ収集の迅速化を目的として、高度医療評価制度が創設された。我々が高度医療に申請を行った新規医療技術「非小細胞肺癌に対するNKT細胞を用いた免疫細胞治療(Chiba-NKT)」は、2011年9月28日に高度医療評価会議にて承認され、2012年1月1日に告示された。
【これまでの実績】
基礎研究
NKT細胞は細胞表面に極めて限定されたT細胞抗原受容体とNKレセプタ−をともに発現しているユニークな細胞である。NKT細胞は抗原提示分子CD1dに提示された糖脂質の1つであるαガラクトシルセラミド(αGalCer)を認識することで特異的に活性化し、殺細胞因子を介して直接の強力な細胞障害活性を発揮する。また迅速にかつ大量に産生されるIFN-γなどのサイトカインを介して、NK細胞やCD8+T細胞といった他のエフェクター細胞の障害活性や樹状細胞に対して調節的役割を果たしている。
マウスモデルにおいて、αGalCerパルス樹状細胞の静脈内投与により、肺内NKT細胞数の増加と、IFN-γ産生の上昇が認められた。マウス肺転移治療モデルにおいては既に成立している小肺転移巣を消失させることが可能であった。またEx vivoでαGalCerにより誘導したヒト活性化NKT細胞は腫瘍に対して直接の細胞障害活性を有することも示された。
臨床研究
(1)αGalCerパルス樹状細胞療法(Phase I 試験)
標準治療終了後の進行・再発非小細胞肺癌に対して、αGalCerパルス樹状細胞の静脈内投与(投与細胞数:5×107/m2、2.5×108/m2、1×109/m2)を施行した。その結果、Grade2を越える有害事象は認めることなくプロトコールを完遂した。最大投与細胞数の全3例における末梢血NKT細胞数の明らかな増加と、NKT細胞からのIFN-γ産生の増強を認めた。腫瘍縮小効果を認めた症例はなく、1例で59ヶ月の生存期間を得た。
(2)αGalCerパルス樹状細胞療法(Phase I-II 試験)
標準治療終了後の進行・再発非小細胞肺癌に対して、1×109/m2のαGalCerパルス樹状細胞の静脈内投与を行った。1例で深部静脈血栓症の再発を認め、Grade3の有害事象と判断された。末梢血単核球のαGalCer反応性IFN-γ産生細胞数の明らかな増加を10例に認めた。全23症例の生存期間中央値は17.4ヶ月であり、またαGalCerパルスDC投与により末梢血単核球中のIFN-γ産生細胞の増加群は、非増加群と比較し有意に全生存期間の延長を認めた(29.3ヶ月対9.7ヶ月、p=0.0011、log-rank test)。
(3)これまでのNKT細胞を利用した肺癌と頭頸部癌の臨床研究のまとめは、Motohashi et al. Clinical Immunology 140:167-76(2011)、「がん免疫療法-実用化へのチャレンジ-」シーエムシー出版(珠玖洋監修)に掲載されている。
【臨床研究実施体制】
千葉大学では、平成24年1月に発足した千葉大学未来医療教育研究センター Future Medicine Research Center (FMRC)(センター長:中山俊憲教授)、大学院医学研究院、医学部附属病院を中心に下図のような研究組織で肺癌と頭頸部癌を対象にしたNKT細胞治療の臨床研究が行われている。

【高度医療の内容】
名称:第3項先進医療(高度医療)
「非小細胞肺癌に対するNKT細胞を用いた免疫細胞治療(Chiba-NKT)
実施責任医師
千葉大学医学部附属病院呼吸器外科 科長 吉野一郎
実施担当医師
千葉大学大学院医学研究院 免疫細胞医学 教授 本橋新一郎
目的
進行・再発非小細胞肺癌の患者に対して、体内でのNKT細胞を活性化するために、αGalCerパルス樹状細胞の静脈内投与を行い、その安全性と有効性を評価する。
適応基準(抜粋)
1) 組織学的もしくは細胞学的に非小細胞癌であることが確認されている
2) 切除不能進行期のstage IIIB/IV期、または術後再発である
3) 非小細胞肺癌に対する化学療法として、初回化学療法が終了している
4) 年齢が20歳以上75歳以下であり、全身状態が良好である
5) 測定可能病変が存在する
6) 登録時に先行治療から4週間以上経過している
7) 主要臓器(骨髄、肝、腎、肺等)の機能が保持されており、以下の基準を満たす
白血球数 3,000/mL以上
血小板数 75,000/mL以上
ヘモグロビン 9.0g/dL以上
血清クレアチン 1.5mg/dL以上
総ビリルビン 1.5mg/dL以上
AST、ALT 2×基準値上限以下
SpO2 (room air) 93%以上
8) 末梢血中にNKT細胞が存在し、一定の基準を満たす
除外基準(抜粋)
1) 重篤な心疾患、肺疾患、感染症、低栄養などの合併症を有する
2) コントロールを必要とする胸水、腹水、心嚢水、脳転移を有する
3) 重複癌を有する
4) ステロイド薬を内服または注射している
5) 自己免疫疾患と診断されている
6) ウィルス感染症(HIV、肝炎等)のキャリア
7) 妊娠中あるいは妊娠の可能性のある女性、および授乳期の女性
治療法
成分採血にて末梢血単核球を採取し、IL-2とGM-CSF存在下に培養する。投与前日にαガラクトシルセラミド(αGalCer)を加えて培養し、培養後7日目、14日目にαGalCerパルス樹状細胞の点滴静注を行う。これを1コースとして、4週間の経過観察後に2コース目を施行する。
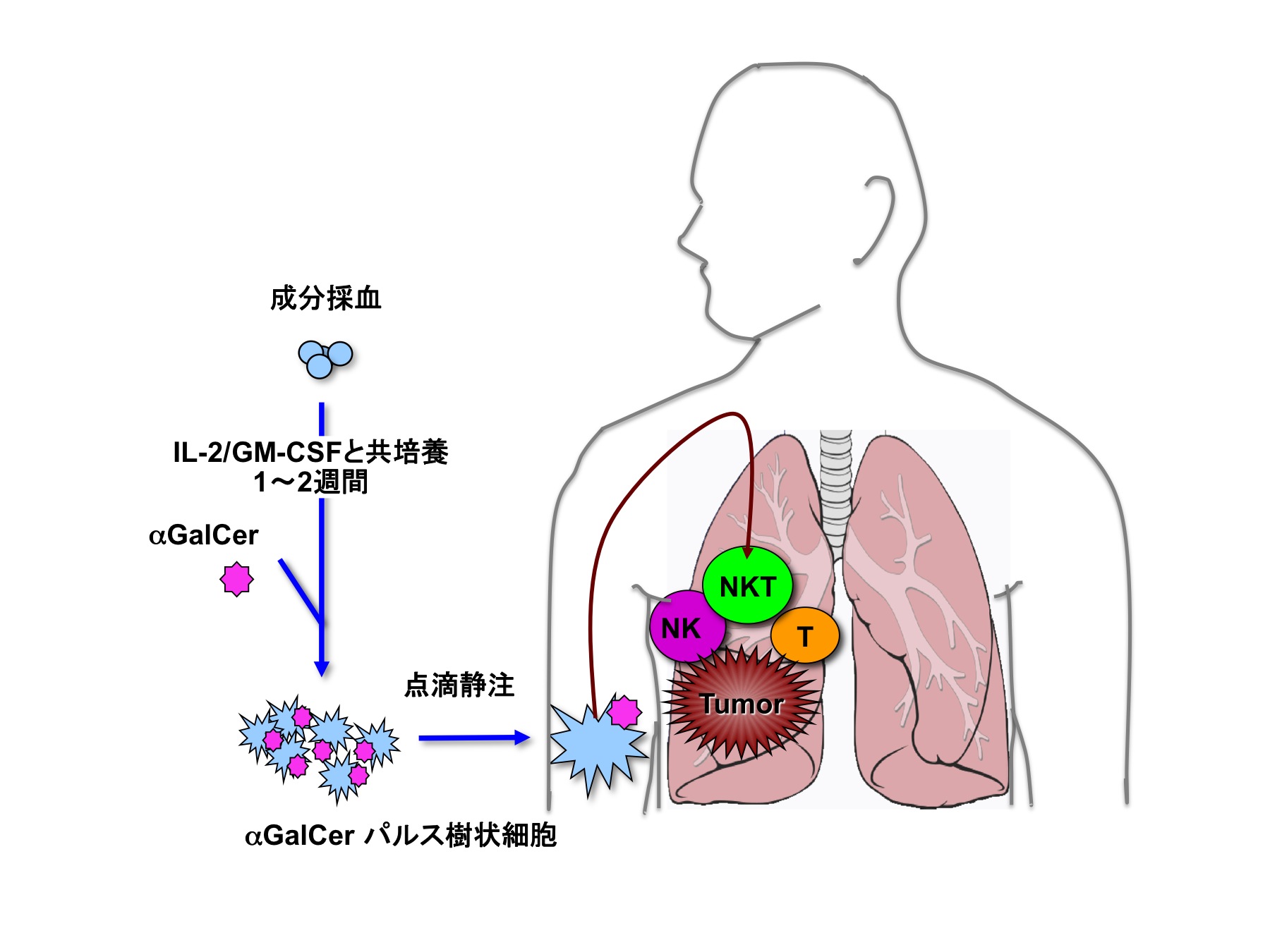
費用
この臨床試験における高度医療に係る分(通常の健康保険が適応されない)は、1コースで約60万円、最大2コース行うと約120万円となる。その他に、通常の保険診療分の費用が必要となる。
問い合わせ先
千葉大学大学院医学研究院 免疫細胞医学 担当:本橋 新一郎
電話番号:043-226-2718(直通)
千葉大学医学部附属病院 呼吸器外科外来
電話番号:043-222-7171(代表)
【参考文献】
- Kawano, T., Cui, J. et al. CD1d-restricted and TCR-mediated activation of Vα14 NKT cells by glycosylceramides. Science 278, 1626-1629 (1997).
- Fujii, S., Motohashi, S.et al. Adjuvant activity mediated by iNKT cells. Semin Immunol 22, 97-102 (2010).
- Akutsu, Y., Nakayama, T. et al. Expansion of lung Vα14 NKT cells by administration of α-galactosylceramide-pulsed dendritic cells. Jpn J Cancer Res 93, 397-403 (2002).
- Motohashi, S., Kobayashi, S. et al. Preserved IFN-γ production of circulating Vα24 NKT cells in primary lung cancer patients. Int J Cancer 102, 159-165 (2002).
- Toura, I., Kawano, T. et al. Cutting edge: inhibition of experimental tumor metastasis by dendritic cells pulsed with α-galactosylceramide. J Immunol 163, 2387-2391 (1999).
- Kawano, T., Nakayama, T. et al. Antitumor cytotoxicity mediated by ligand-activated human Vα24 NKT cells. Cancer Res 59, 5102-5105 (1999).
- Ishikawa, A., Motohashi, S. et al. A phase I study of α-galactosylceramide (KRN7000)-pulsed dendritic cells in patients with advanced and recurrent non-small cell lung cancer. Clin Cancer Res 11, 1910-1917 (2005).
- Motohashi, S., Nagato, K. et al. A phase I-II study of α-galactosylceramide-pulsed IL-2/GM-CSF-cultured peripheral blood mononuclear cells in patients with advanced and recurrent non-small cell lung cancer. J Immunol 182, 2492-2501 (2009).
- Motohashi, S., Okamoto, Y. et al. Anti-tumor immune responses induced by iNKT cell-based immunotherapy for lung cancer and head and neck cancer. Clin Immunol 140, 167-76 (2011).
