研究テーマ

千葉大学大学院医学研究院
呼吸器病態外科学
千葉大学病院
呼吸器外科

現在の原発性肺癌に対する術前診断や手術の方法では、たとえ他臓器に転移がなく完全に取りきることが可能と判断されて手術に臨んでも、その半数以上に術後再発や転移が発見されます。この再発を抑制することが肺癌の治療成績向上には不可欠なことです。
この再発や転移を抑制することの一つの方法として、これまで免疫療法が考案されてきました。それは肺癌の患者では何らかの免疫力低下の存在が指摘されており、肺癌手術後の効果的な免疫療法が免疫力を回復させることで残存する腫瘍の増殖を抑制し、延命効果をもたらすことが期待されてきたからです。この免疫力の低下をもたらす因子は腫瘍から直接放出されているものもあり、腫瘍を切除する手術療法も広い意味で免疫療法の一つと言えるかもしれませんが、もっと積極的に免疫反応に介入して、抗腫瘍効果を高めるような免疫賦活作用を誘導する免疫療法の開発・研究を行ってきました。
千葉大学大学院医学研究院胸部外科学教室では前身の千葉大学肺癌研究施設外科部門であった1960年代に施行された肺癌に対する長期間歇化学療法の経験をふまえて、1970年代には受動免疫療法の一つとしてリンパ球から抽出した因子であるtransfer factor による術後免疫療法を中心とした無作為比較試験を行いました。さらに1980年代には手術時に得られたリンパ節のリンパ球および末梢血のリンパ球から誘導したLAK(lymphokine activated killer cell)にT細胞増殖因子であるInterleukin-2を加えた養子免疫療法の無作為比較試験を行い、術後免疫化学療法の有効性を示してきました。
このような原発性肺癌に対する免疫療法の当教室における流れの中で、千葉大学大学院免疫発生学谷口克教授の研究室にて精力的に研究が進められていたNKT細胞を標的とした免疫細胞療法に関する共同研究が1990年代後半からスタートしました。
NKT細胞とは同一の細胞表面にT細胞レセプターとNK細胞レセプターをともに発現しているユニークなリンパ球であり、T細胞、B細胞、NK細胞とは区別される第4のリンパ球として報告されました。NKT細胞はNK受容体とともにマウスではVα14Jα18遺伝子、ヒトではVα24Jα18遺伝子でコードされる均一なT細胞抗原受容体(TCR)を発現していることを特徴とし、特に免疫調節において重要な役割を担っています。NKT細胞のTCRで認識される抗原として、抗原提示細胞上のCD1d分子に提示された糖脂質のα-ガラクトシルセラミド(αGalCer)があります。αGalCerによる活性化後、さまざまな殺細胞誘導因子を発現することで標的細胞に対して直接細胞傷害活性を示します。さらに樹状細胞の成熟化を進め、NK細胞や細胞傷害性T細胞(CTL)の有する細胞傷害活性をより強力にするといったアジュバント効果を持つ非常にユニークな細胞です。
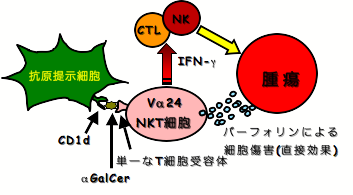
図1:NKT細胞の抗腫瘍メカニズム
αGalCerをマウスの悪性腫瘍転移モデルに対してin vivoに単独で投与すると、NKT細胞が活性化し顕著な転移抑制効果を示しますが、αGalCerをex vivoで調製した樹状細胞に提示させた形で投与するとさらに腫瘍増殖抑制効果が増強されることを報告されてきました。この方法ではすでに形成された微小転移巣を消失させることができるほどの強い抗腫瘍効果を示すことが可能です。また、NKT細胞免疫系は種属においてCD1d分子-NKT細胞抗原受容体が共通であるため、誰のNKT細胞であってもαGalCerによって活性化することが可能です。さらに活性化したNKT細胞は腫瘍細胞における抗原性変異やMHCクラスI分子の発現の強弱には影響を受けにくいと予測されます。この点が、癌細胞上のMHC分子と結合した癌特異的ペプチド抗原を標的としたCTLを利用した細胞免疫療法との大きな差異です。多くの腫瘍細胞でMHCの発現低下がみられる場合にはCTLから逃れ、免疫回避の主な理由ともなっていたからです。
原発性肺癌に対してin vivoでのNKT細胞免疫系の活性化を目指すαGalCer パルス樹状細胞療法を施行しました。まず末梢血より成分採血にてリンパ球を採取し、サイトカインと共培養して分化誘導した樹状細胞を含む細胞分画にαGalCerをパルスし提示させた後、患者本人へ静脈内投与にて戻します。計17例の手術不能進行期肺癌症例もしくは肺癌術後再発症例の標準治療を行った後に、1回当たり1×109個のαGalCerパルス樹状細胞を計4回静脈内投与しました。その結果、細胞投与に関連する重篤な副作用や有害事象を認めることなく施行可能であることが確認できました。αGalCerパルス樹状細胞投与後のNKT細胞特異的免系学的解析を進め、NKT細胞特異的なIFN-γ産生増強が樹状細胞治療後の生存期間延長に重要であることが判明しました。
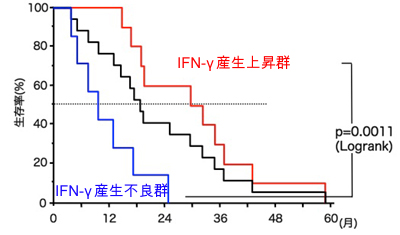
図2:αGalCerパルス樹状細胞投与後の全生存曲線
原発性肺癌に対して体外で活性化したNKT細胞を投与する活性化NKT細胞療法を施行しました。投与NKT細胞数を1x107/m2および5x107/m2と設定し、安全性の確認およびNKT細胞特異的免疫反応の検出及び抗腫瘍効果の判定を行いました。結果として、観察期間中に重篤な有害事象は認められず、NKT細胞特異的免疫学的反応の検討では、活性化NKT細胞投与とともに末梢血中のαGalCer反応性のIFN-γ産生細胞数の上昇を認めました。
原発性肺癌に対し、より効率よく免疫反応を誘導する方法として、気管支鏡下に腫瘍本体またはリンパ節にαGalCerパルス樹状細胞を投与する局所免疫療法の安全性と有効性について検討を行いました。観察期間中、細胞治療に関連する重篤な有害事象は認められず、末梢血NKT細胞数やIFN-g産生細胞数の増加を認めた症例も得られ、現在更なる詳細な解析を行っております。
現在、aGalCerパルス樹状細胞療法の有効性や安全性を検討することを目的とした新規臨床研究「切除不能進行期ならびに再発非小細胞肺癌に対するa-ガラクトシルセラミドパルス樹状細胞を用いた免疫細胞治療」を行っております。本臨床試験は科学的根拠に基づき一定の効果や安全性を期待でき、適切な計画と方法がとられている臨床試験として厚生労働省に高度医療として承認されました。詳細につきましては、本ホームページのトップページにあります「治療法について」の項目から、「新しい臨床研究に関するお知らせ」をご参照下さい。
お問い合わせ:千葉大学医学部附属病院 未来開拓センター
電話 043-226-2718(研究室直通)